Cours simple : Décroissance radioactive pour le terminale : Lycée Bac
I- Le noyau atomique
1-Structure de l’atome
L’atome est formé d’un nuage électronique entourant d’un noyau central.
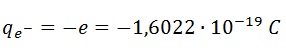
Le noyau est chargé positivement d’une charge égale et opposée en signe à celle du nuage électronique.
2-Composition du noyau
Le noyau atomique est composé de particules appelées nucléons( protons et neutrons). Les protons sont des particules chargées positivement avec la charge élémentaire

Les neutrons sont des particules portant une charge neutre.
3-Élément chimique
Un élément chimique est l’ensemble des atomes ou ions monoatomiques portant le même nombre de protons dans leur noyau.
Sa représentation symbolique est la suivante:

4-Le nucléide
Un nucléide : espèce qui se différencie des autres, soit par son nombre de nucléons A (protons et neutrons)., soit par de nombre de charge Z.
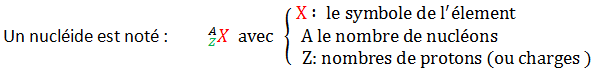
- X est le symbole de l’élément
- A: nombre de masse et représente le nombre de nucléons (protons et neutrons).
- Z : nombre de charge et représente le nombre de protons
Le nombre de neutrons N est donné par :
N : nombre de neutrons se détermine par l’expression : N=A−Z .
Exemple:
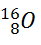
- Elément oxygène
- Nombre de protons Z=8
- Nombre de nucléons A=16
- Nombre de neutrons N=A−Z=8
- Nom du nucléide Oxygène 16

5-Les isotopes
Deux nucléides sont dits isotopes s’ils ont même nombre de protons.
Exemple :

6-Diagramme de Ségré (N,Z)
Il existe deux types de noyaux :
Noyaux stables : conservent toujours la même structure
Noyaux instables : ou noyaux radioactifs se transforment spontanément à d’autres noyaux avec émission de rayonnement.
Le diagramme de Ségré indique :

- Les Noyaux stables
- Noyaux instables ou noyaux radioactifs
- Fournit le type d’émission radioactive.
Les axes sont :
- en abscisse : le nombre de neutrons N = A – Z
- en ordonnée : le nombre de protons : Z
Pour Z < 20 les noyaux stables se situent au voisinage de la droite N=Z . Leurs nombres de neutrons et de protons sont donc égaux

Pour Z>20 les noyaux stables se situent au dessus de la droite N=Z donc leur nombre de neutrons est supérieur à leur nombre de protons.
On observe que les noyaux stables ont un nombre N égal ou légèrement supérieur au nombre Z, situés dans une zone centrale appelé la vallée de stabilité .
Aucun noyau dont Z>82 n’est stable.
Les noyaux radioactifs se désintègrent en se rapprochant de la courbe de stabilité après l’émission de rayonnements radioactifs énergétiques :
- Les noyaux dont le nombre de protons est trop grand sont du type émetteur bêta plus (β+)
- Les noyaux dont Z est trop faible sont du type émetteur bêta moins (β–)
- Les noyaux lourds avec un excès de protons sont des émetteurs alpha (α)
II – La radioactivité
1-Définitions de la radioactivité
Un noyau radioactif est un noyau instable qui se désintègre spontanément en émettant une particule.
La radioactivité est une désintégration naturelle d’un noyau radioactif à un noyau fils plus stable avec émission d’une particule.
2-Propriétés de la radioactivité
- La désintégration radioactive est un phénomène :
Aléatoire : aucune prévision d’une désintègre d’un noyau radioactif
Spontané : elle se déclenche seule, sans intervention extérieure ; indépendant de la température, de la pression,…ect.
3- Lois de conservation :
Les transformations nucléaires obéissent à des lois de conservation, appelées lois de conservation de Soddy : Au cours des transformations nucléaires, il y a conservation du nombre de charge Z et du nombre de nucléons A.
- Un noyau père (X) donne naissance à un noyau fils (Y) en émettant une particule P chargée :
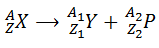
Les lois de conservation s’écrivent :

4- Les différents types d’émissions radioactives :
On distingue 3 types de radioactivité :
- alpha α : la particule est un noyau d’hélium 24He
- bêta moins β– : la particule émise est un électron -10e
- bêta plus β+ : la particule est un positron +10e
Radioactivité alpha α
La radioactivité 𝜶 est une désintégration nucléaire naturelle spontanée correspond aux noyaux lourds (A > 200) dans laquelle un noyau père transforme en un noyau fils avec l’émission d’un noyau d’Hélium
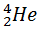


b) Radioactivité β–
La radioactivité b– correspond à l’émission d’électrons.
C’est une désintégration nucléaire naturelle spontanée correspond aux noyaux en excès de neutrons (situés au dessus de la courbe de stabilité) dans laquelle un noyau père transforme en un noyau fils avec l’émission d’un électron.

Cela provient de la décomposition d’un neutron en un proton et électron suivant l’équation :
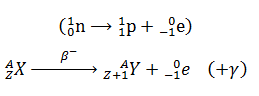
C) Radioactivité β+
La radioactivité b+ correspond à l’émission de positrons

C’est une désintégration nucléaire naturelle spontanée correspond aux noyaux en excès de protons, (situés en dessous de la courbe de stabilité) dans laquelle un noyau père se transforme en un noyau fils avec l’émission d’un positron,cela provient de la décomposition d’un proton en neutron et un positron suivant l’équation :
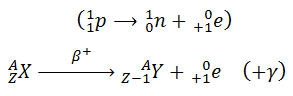

D) Le rayonnement y
Le rayonnement y est une onde électromagnétique de très grande énergie, émis au cours des désintégrations α et β– et, β+ le noyau fils est produit dans un état excité (ayant un excès d’énergie par rapport à son état fondamental).
Ce noyau libère un rayonnement Y selon l’équation suivante :

Remarque :
Un noyau dans un état excité est représenté avec un astérisque (*) en exposant à droite
Exemple :
Émission Y associée à la radioactivité α
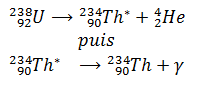
5- Familles radioactives
La radioactivité entraîne la transformation d’un nucléide en un autre nucléide. Si ce dernier est lui-même radioactif, il se transforme continuellement, et ainsi de suite jusqu’à ce que le nucléide obtenu soit stable La famille radioactive est l’ensemble des nucléides obtenus à partir d’un même noyau père
Exemple:

Il existe quatre familles radioactives naturelles provenant des noyaux suivants :

III – Loi de décroissance radioactive
La radioactivité est un phénomène aléatoire spontané, imprévisible dans le temps . L’évolution dans le temps d’un échantillon radioactif est soumise à une loi statistique appelée loi de décroissance radioactive (découvert par Rutherford et Soddy en 1902).
1- Loi de décroissance radioactive
Soit N0 le nombre de noyaux radioactifs initialement présents (à l’instant t=0)
Soit N(t) le nombre de noyaux radioactifs présents à un instant t quelconque restants (non désintégrés).
le nombre de noyaux diminue au cours du temps donc à l’instant t+dt :
Nt+dt – Nt = dN(t) <0 ) donc (– dN(t)>0) nombre de noyaux radioactifs disparus (désintégrés) pendant une durée très brève dt
Les expériences ont confirmé que −dN(t)est proportionnelle à N(t) et dt.
C-à-d – dN(t)= l.N(t).dt en fin dN(t)= -l.N(t).dt
l est la constante radioactive, qui dépend de la nature du noyau radioactif, l représente la proportion de noyaux qui se désintègre par unité de temps elle s’exprime en s-1 .
Note : l = Landa = Constante radioactive

A l’instant t=0 on a N(0)= N =ec =N0
Par conséquent, nous exprimons la loi de décroissance radioactive d’un échantillon radioactif comme suit :
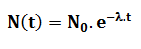
Avec
- N0 le nombre de noyaux initialement présents dans l’échantillon
- N(t) le nombre de noyaux radioactifs encore présents à l’instant
- l représente la constante radioactive en s-1 , propre au corps considéré
2- Constante de temps

La constante de temps, notée τ d’un élément radioactif est l’inverse de la constante radioactive. Elle s’exprime en s à la date.


3-Temps de demi-vie
La demi-vie t1/2 d’un échantillon de noyaux radioactifs est la durée au bout de laquelle la moitié des noyaux initialement présents se sont désintégrés.


La demi-vie est une constante caractéristique d’un élément radioactif.

4- Activité d’un échantillon radioactif
Définition L’activité a(t) d’une source contenant N noyaux radioactifs à la date t est égale au nombre de noyaux qui se désintègrent chaque seconde.

a(t) se mesure en becquerel Bq, ( 1 Bq correspond à 1 désintégration par seconde ).
Évolution de l’activité
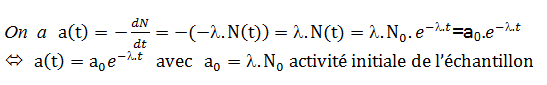
5-Datation radioactive
Dans l’atmosphère, les particules (neutrons) cosmiques entrent en collision avec des atomes d’azote. Au cours de ce choc, l’atome d’azote perd un proton et se transforme en carbone 14.
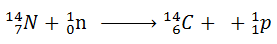
Le carbone radioactif se lie avec de l’oxygène pour former du dioxyde de carbone qui est échangé avec le monde vivant (respiration par les plantes, grâce à la photosynthèse, alimentation et respiration des organismes vivants. Aussi longtemps qu’un organisme vivants vit encore, il continue de prélever du C14, dont la proportion reste fixe :
(1 atome de C14 pour 750 milliards d’atomes de C12)
- Pendant toute leur vie, la proportion de carbone 14 reste constante.
- Dès qu’un organisme meurt, le carbone 14 qu’il contient n’est plus renouvelé puisque les échanges avec le monde extérieur cessent, sa proportion se met à décroître selon l’équation :

On mesure l’activité a(t) d’une masse d’échantillon connue, et connaître a0 l’activité de la même masse d’un échantillon témoin existant. Alors, on peut déterminer son âge t par la relation suivante :

Et on a arrivé à la fin du cours : Décroissance radioactive.







